当降临人世不到1年的婴儿被诊断出严重威胁生命的癌症,对于整个家庭,无疑是一个晴天霹雳。但令人费解的是,其中一些患儿的病症会出现神奇的变化:在不接受治疗的情况下,他们体内的肿瘤也会自行消失。
这些孩子患上的,是一种极为凶险而常见的肿瘤——神经母细胞瘤。这是婴幼儿中最常见的颅外实体肿瘤,在癌症导致的婴幼儿病例中,有15%都是神经母细胞瘤导致的。
这类肿瘤的来源要追溯到胚胎发育期,形成于未分化的交感神经节细胞。因此,在肾上腺、脊柱、颈部、胸部和腹部这些有交感神经节的部位,神经母细胞瘤都有可能出现。随后,肿瘤可以转移至身体多个部位,并发展出对化疗的耐药性。
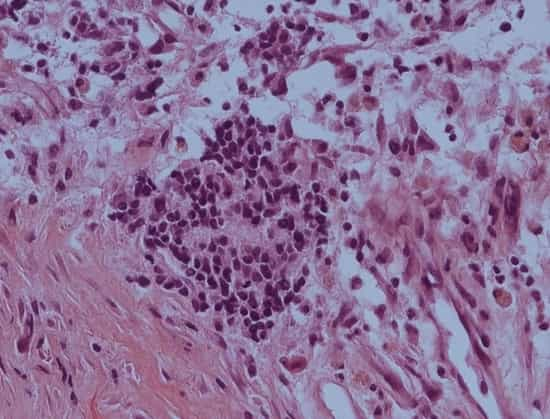
▲侵袭性的神经母细胞瘤细胞在组织中聚集(图片来源:参考资料[2];Credit:Frank Westermann/DKFZ)
结果就是,对于相当一部分高危的神经母细胞瘤患儿,即使接受高强度治疗,但也难以长期有效地控制肿瘤。很多孩子还没来得及感受世界的美好,就被癌症夺走了生命。
然而,在神经母细胞瘤患儿中,却有一小部分幸运儿。他们即使不接受任何治疗,肿瘤竟然也会自行消失。为什么同样是神经母细胞瘤,在不同患儿身上的差异会如此巨大?
在一项发表于《自然·癌症》的研究中,来自德国癌症研究中心(DKFZ)等机构的科学家向这个问题发起了挑战。他们发现,一种氨基酸的缺失或许能解释这些患儿癌细胞的消失。

这项发现要从一种近期备受关注的癌基因家族成员——MYCN基因说起。最近有研究指出,作为疾病发展方向的调控因素,MYCN基因决定了前体细胞是否会发展成为成熟的神经细胞,或是演变为恶性的神经母细胞瘤。
恶性神经母细胞瘤的基因组中,携带了数百个活跃的MYCN基因的拷贝,其高度活跃导致了癌细胞代谢的大幅转变。但问题在于,这种基因到底给癌细胞带来了怎样的好处?如果能终止MYCN基因的作用过程,那么癌症的进程是否也能得到遏制?
基于这样的思路,研究团队对MYCN基因在神经母细胞瘤中的作用进行了研究。他们发现,MYCN高度活跃的神经母细胞瘤细胞对半胱氨酸有着格外旺盛的需求。
对于大多数细胞,半胱氨酸都是蛋白质和脂质的重要构造单元。而快速增殖的癌细胞显然需要这些蛋白质与脂质来生产新细胞。
另一方面,癌细胞也需要半胱氨酸来保护自己,清除高度活跃的代谢产生的大量过氧化物毒素。而当神经母细胞瘤细胞缺乏半胱氨酸时,它们会通过两种途径来获取:使用宿主摄入的氨基酸,或是利用甲硫氨酸,通过另一条合成路径来生产半胱氨酸。
神经母细胞瘤细胞对半胱氨酸的依赖,让研究团队想到:如果人为剥夺了半胱氨酸,在MYCN驱动的肿瘤细胞内部,过氧化物毒素将开始积累,导致细胞铁死亡。因此,半胱氨酸或许就是恶性神经母细胞瘤的阿喀琉斯之踵。
为了验证这样的猜想,在小鼠实验中,研究团队阻断了半胱氨酸的摄入与合成途径,并且让一类用于消耗过氧化物的酶失活。这时,由于过氧化物的大量积累,癌细胞就能通过铁死亡启动自我毁灭程序,肿瘤也随之缩小。
这项研究首次在患癌小鼠体内证实,铁死亡可以用于杀死高度侵袭性的神经母细胞瘤细胞。
同样是这个过程,或许解释了部分神经母细胞瘤患儿癌细胞的自行消失。“在生命的第一年,细胞获取的半胱氨酸通常较少。因此,当这些细胞开始不受控地分裂,它们的半胱氨酸储库很快清空,因此铁死亡也就启动了。”论文共同通讯作者Hamed Alborzinia博士解释道。一些MYCN不活跃的神经母细胞瘤无法摆脱自我清除的结局,在半胱氨酸缺失到一定阶段时死去。
而对于那些MYCN基因高度活跃的高风险患者,这项研究为半胱氨酸摄入、生产与消耗的平衡提供了新的理解,也为更多研究者提供了启动癌细胞自我销毁过程的新思路。我们期待通过未来的临床试验,这一过程将真正用于治疗神经母细胞瘤患儿,让那些不幸的患儿健康成长、感受世界的美好。